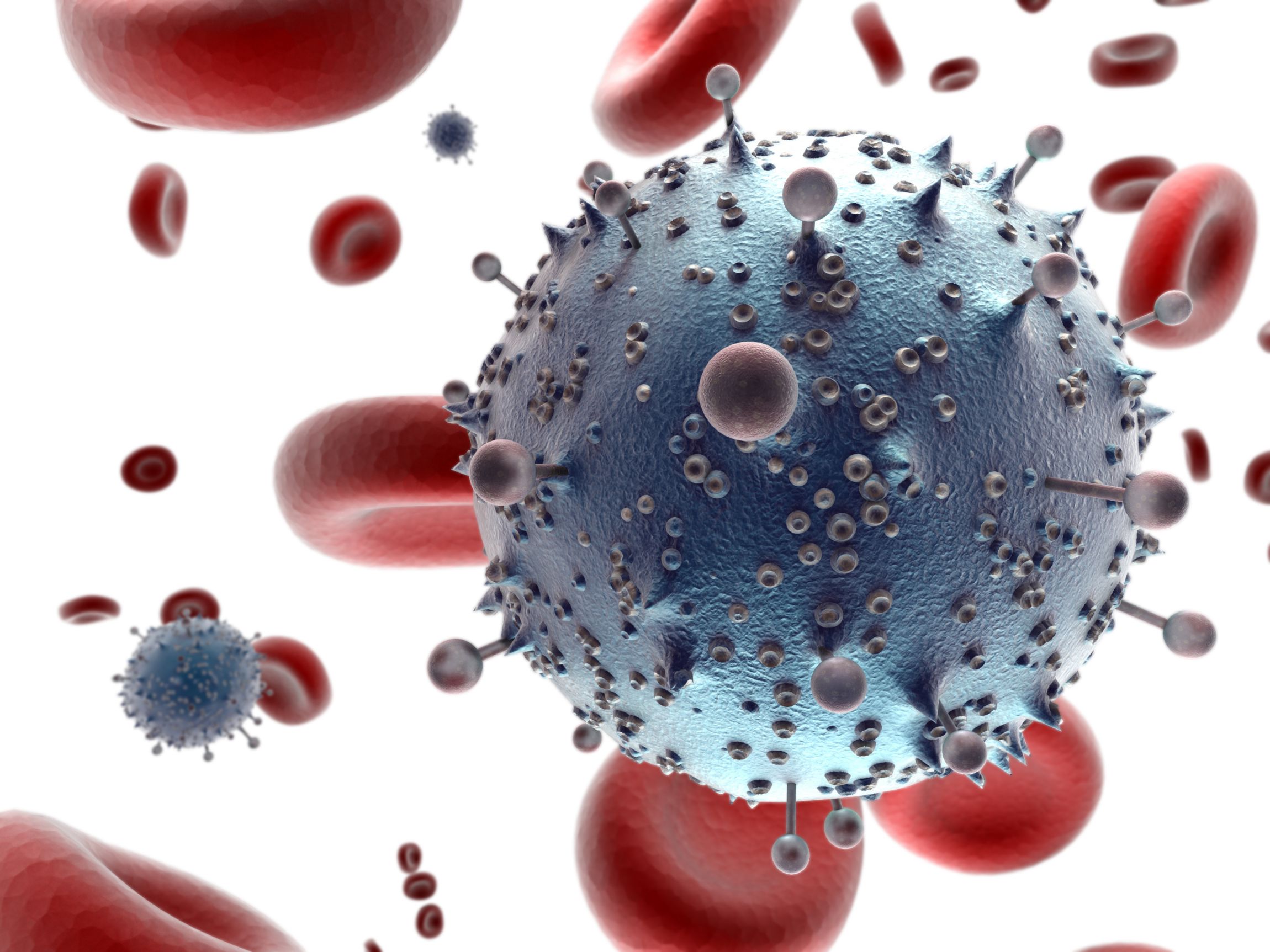
O que é AIDS?
Em 1981, a vigilância epidemiológica dos EUA detectou aumentos significativos e absolutamente inesperados em certas doenças incomuns, porém típicas de portadores de imunodepressão avançada, como a pneumonia pelo Pneumocystis jíroveci (antigo P caríníí) e o sarcoma de Kaposí. Em 1983 o vírus da imunodeficiência humana (HIV) foi isolado e em 1984 sua relação causal com a AIDS estabelecida. Pronto, estavam de frente com uma doença epidêmica de característica global, dinâmica e instável, cuja forma de ocorrência depende, entre outros determinantes, do comportamento humano individual e coletivo.
Quem é o agente?
O HIV é um retrovírus citopático e não-oncogênico. Morfologicamente, o HIV é uma partícula icosaédrica de cuja superfície despontam espículas formadas por glicoproteínas (gp 120 e gp 41). O HIV contém ainda um capsídeo (envelope interno) composto pelo antígeno p24. Dentro do capsídeo estão encerrados o genoma viral (RNA) e enzimas como a transcriptase reversa. Há dois tipos principais do vírus: HIV-1 e HIV-2. Cada tipo é dividido em grupos: M, N, P e O para o HIV-1; de A a G para o HIV-2. Cada grupo, por sua vez, é subdividido em “clades”, em função de pequenas diferenças genéticas. Por que isso é importante? As “clades” podem se recombinar entre si caso o paciente for infectado por 2 ou mais vírus diferentes, originando as formas recombinantes circulantes ou CRF´s.
Como é o ciclo vital do HIV na célula humana?
- ligação de glicoproteínas virais (gp120) ao receptor específico da superfície celular (principalmente linfócitos T-CD4). Essa interação entre gp120 e CD4 promove a mudança conformacional que expõe o sítio de ligação de um correceptor (CCR5 e CXCR4). A ligação do correceptor, por sua vez, produz mais uma mudança conformacional que leva à exposição da gp 41 (que estava “escondida” embaixo da gp 120).
- fusão do envelope do vírus com a membrana da célula hospedeira através da gp41;
- liberação do “core” do vírus para o citoplasma da célula hospedeira;
- transcrição do RNA viral em DNA complementar, dependente da enzima transcriptase reversa;
- transporte do DNA complementar para o núcleo da célula, onde pode haver integração no genoma celular (provírus), dependente da enzima integrase, ou a permanência em forma circular, isoladamente;
- o provírus é reativado, e produz RNA mensageiro viral, indo para o citoplasma da célula;
- proteínas virais são produzidas e quebradas em subunidades, por intermédio da enzima protease;
- as proteínas virais produzidas regulam a síntese de novos genomas virais, e formam a estrutura externa de outros vírus que serão liberados pela célula hospedeira; e
- o vírus recém-formado é liberado para o meio circundante da célula hospedeira, podendo permanecer no fluído extracelular, ou infectar novas células. Porque é importante saber sobre o ciclo viral? A interferência em qualquer um destes passos do ciclo vital do vírus impediria a multiplicação e/ou a liberação de novos vírus. Atualmente estão disponíveis comercialmente drogas que interferem em duas fases deste ciclo: a fase 4 (inibidores da transcriptase reversa) e a fase 7 (inibidores da protease).
Quais são as formas de transmissão?
- sexual;
- sanguínea (em receptores de sangue ou hemoderivados e em usuários de drogas injetáveis);
- vertical (da mãe para o filho, durante a gestação, parto ou por aleitamento).
Além dessas formas, mais frequentes, também pode ocorrer a transmissão ocupacional, ocasionada por acidente de trabalho, em profissionais da área da saúde que sofrem ferimentos com instrumentos pérfuro-cortantes contaminados com sangue de pacientes infectados pelo HIV.
Como é a história natural da doença?
A doença causada pelo HIV é essencialmente caracterizada por uma queda progressiva na contagem de linfócitos T CD4+ (linfócitos T helper). A perda dessas células – que têm o papel de “maestros” do sistema imune – resulta no aparecimento de infecções e neoplasias oportunistas, culminando num estado de profunda imunodeficiência. Diversos são os modos pelos quais o HIV compromete os linfócitos T CD4+. Ocorre destruição direta pela replicação viral (efeito citopático), mas também destruição indireta mediada pelo próprio sistema imune do hospedeiro, que reconhece e agride as células infectadas (ex.: citotoxicidade de linfócitos T CD8+, células natural killer e anticorpos anti-HIV). Ocorrem ainda os fenômenos de “exaustão celular” ou anergia (disfunção qualitativa) e apoptose (morte celular programada), ambos desencadeados pela ativação imune exagerada.
Como controlar e prevenir?
As principais estratégias de prevenção empregadas pelos programas de controle envolvem: a promoção do uso de preservativos, a promoção do uso de agulhas e seringas esterilizadas ou descartáveis, o controle do sangue e derivados, e manejo adequado das outras DST. Quando falando em cuidados na exposição ocupacional a material biológico, a prevenção baseia-se na utilização sistemática das normas de biossegurança, no uso de precauções universais (luvas, óculos de proteção, máscaras, aventais, etc.), na determinação dos fatores de risco associados, e na sua eliminação, bem como na implantação de novas tecnologias da instrumentação usadas na rotina de procedimentos invasivos.
AIDS e a Odontologia
É importante ressaltar que muitas vezes os primeiros sinais clínicos da imunodeficiência associados ao HIV aparecem na cavidade oral, o que pode possibilitar ao cirurgião-dentista um papel relevante no diagnóstico precoce da infecção pelo HIV e no tratamento desse grupo de pacientes. Assim sendo, o cirurgião-dentista pode ser o primeiro profissional de saúde a reconhecer os sinais e sintomas causados pela presença do vírus no organismo porque muitos indivíduos infectados desconhecem sua condição. Sempre que houver suspeita de infecção pelo HIV, o cirurgião-dentista deve solicitar o diagnóstico sorológico e encaminhar o paciente ao infectologista para exames complementares e tratamento adequado. Com relação aos pacientes já diagnosticados, as normas universais de biossegurança, que são importantes para evitar contaminação, devem ser adotadas como rotina em todo e qualquer atendimento. Todas as medidas de proteção da equipe e o do paciente devem ser praticadas indiscriminadamente, como o uso dos equipamentos de proteção individual e esterilização por meio de autoclave.
Como diagnosticar?
A infecção pelo HIV é geralmente confirmada por meio da sorologia. Este método permite demonstrar a presença de anticorpos contra antígenos virais no soro (ex.: anti-p24, anti-gp41, anti-gp120) e/ou a presença dos antígenos em si (ex.: antigenemia p24). Os anticorpos anti-HIV aparecem, em média, dentro de 4 semanas após a infecção primária. Enquanto antígenos virais ou anticorpos anti-HIV não tiverem surgido no soro do paciente, diremos que ele se encontra no período de janela imunológica. Podemos separar em duas fases: (1)Triagem: Inicialmente, utilizam-se testes sorológicos de altíssima sensibilidade (baixa chance de falso-negativo), o que detecta quase 100% dos infectados. O teste de triagem mais usado na prática é o ELISA anti-HIV, que detecta apenas anticorpos, é de baixo custo, e possui sensibilidade elevada (>99,5%). (2)
- Confirmação: Esta etapa lança mão de testes de alta especificidade (baixa chance de falso-positivo), com o intuito de definir os pacientes positivos na primeira etapa que representam, de fato, “verdadeiros-positivos”. Os testes de alta especificidade em geral são mais caros e menos sensíveis, o que inviabiliza seu emprego como testes de triagem. Segundo os americanos, o teste de escolha para confirmação diagnóstica é o Western Blot, um método de altíssima especificidade (em torno de 99,7%). Definições de AIDS no Brasil Critério CDC adaptado Positividade em 2 testes de triagem ou 1 teste confirmatório para detecção de anticorpos anti-HIV + Evidência de imunodeficiência: diagnóstico de pelo menos 1 doença indicativa de AIDS e/ou CD4 < 350cél/mm3 A contagem de células T CD4+ em sangue periférico tem implicações prognósticas na evolução da infecção pelo HIV, pois é a medida de imunocompetência celular; é útil no acompanhamento de pacientes infectados pelo HIV. De maneira didática pode-se dividir a contagem de células T CD4+ em sangue periférico em quatro faixas: – maior que 500 células/mm3: estágio da infecção pelo HIV com baixo risco de doença. Casos de infecção aguda podem apresentar estes níveis de células T CD4+. – entre 200 e 500 células/mm3: estágio caracterizado por surgimento de sinais e sintomas menores ou alterações constitucionais. Risco moderado de desenvolvimento de doenças oportunistas. Nesta fase, podem aparecer candidíase oral, herpes simples recorrente, herpes zoster, tuberculose, leucoplasia pilosa, pneumonia bacteriana. – entre 50 e 200 células/mm3: estágio com alta probabilidade de surgimento de doenças oportunistas como pneumocistose, toxoplasmose de SNC, neurocriptococose, histoplasmose, citomegalovirose localizada. Está associado à síndrome consumptiva, leucoencefalopatia multifocal progressiva, candidíase esofagiana. – menor que 50 células/mm3: estágio com grave comprometimento de resposta imunitária. Alto risco de surgimento de doenças oportunistas como citomegalovirose disseminada, sarcoma de Kaposi, linfoma não-Hodgkin e infecção por micobactérias atípicas.
Quais são os aspectos clínicos?
A infecção pelo HIV pode ser dividida em quatro fases clínicas:
- infecção aguda;
- fase assintomática, também conhecida como latência clínica;
- fase sintomática inicial ou precoce;
- AIDS – Infecção aguda
A infecção aguda, também chamada de síndrome da infecção retroviral aguda ou infecção primária, ocorre em cerca de 50% a 90% dos pacientes. Seu diagnóstico é pouco realizado devido ao baixo índice de suspeição. O tempo entre a exposição e os sintomas é de cinco a 30 dias. A história natural da infecção aguda caracteriza-se tanto por viremia elevada, como por resposta imune intensa. Durante o pico de viremia, ocorre diminuição rápida dos linfócitos T CD4+, que posteriormente aumentam, mas geralmente não retornam aos níveis prévios à infecção. Os sintomas aparecem durante o pico da viremia e da atividade imunológica.
As manifestações clínicas podem variar desde quadro gripal até uma síndrome mononucleose-like. Além de sintomas de infecção viral, como febre, adenopatia, faringite, mialgia, artralgia, rash cutâneo maculopapular eritematoso, ulcerações mucocutâneas envolvendo mucosa oral, esôfago e genitália, hiporexia, adinamia, cefaléia, fotofobia, hepatoesplenomegalia, perda de peso, náuseas e vômitos; os pacientes podem apresentar candidíase oral, neuropatia periférica, meningoencefalite asséptica e síndrome de Guillain-Barré. Após a resolução da fase aguda, ocorre a estabilização da viremia em níveis variáveis. Fase assintomática na infecção precoce pelo HIV, também conhecida como fase assintomática, o estado clínico básico é mínimo ou inexistente.
Fase sintomática inicial – sudorese noturna: Pode ser recorrente e pode ou não vir acompanhada de febre; – Fadiga: referida como mais intensa no final de tarde e após atividade física excessiva; – Emagrecimento: Geralmente encontra-se associado a outras condições como anorexia. A associação com diarreia aquosa o faz mais intenso; – Diarreia: consiste em manifestação frequente da infecção pelo HIV desde sua fase inicial. Determinar a causa da diarreia pode ser difícil e o exame das fezes para agentes específicos se faz necessário; – Sinusopatias: Febre, cefaleia, sintomas locais, drenagem mucopurulenta nasal fazem parte do quadro; – Candidíase Oral e Vaginal (inclusive a recorrente): a candidíase oral é a mais comum infecção fúngica em pacientes portadores do HIV e apresenta-se com sintomas e aparência macroscópica característica. A forma pseudomembranosa consiste em placas esbranquiçadas removíveis em língua e mucosas que podem ser pequenas ou amplas e disseminadas. Já a forma eritematosa é vista como placas avermelhadas em mucosa, palato mole e duro ou superfície dorsal da língua. A queilite angular, também frequente, produz eritema e fissuras nos ângulos da boca;
- Leucoplasia Pilosa Oral: é um espessamento epitelial benigno causado provavelmente pelo vírus Epstein-Barr, que clinicamente se apresenta como lesões brancas que variam em tamanho e aparência, podendo ser planas ou em forma de pregas, vilosidades ou projeções. Ocorre mais frequentemente em margens laterais da língua, mas podem ocupar localizações da mucosa oral: mucosa bucal, palato mole e duro;
- Gengivite: a gengivite e outras doenças periodontais pode manifestar de forma leve ou agressiva em pacientes com infecção pelo HIV, sendo a evolução rapidamente progressiva, observada em estágios mais avançados da doença, levando a um processo necrotizante acompanhado de dor, perda de tecidos moles periodontais, exposição e sequestro ósseo;
- Úlceras Aftosas: presença de úlceras consideravelmente extensas, resultantes da coalescência de pequenas úlceras em cavidade oral e faringe, de caráter recorrente e etiologia não definida;
- Herpes Simples Recorrente: a maioria dos indivíduos infectados pelo HIV é coinfectada com um ou ambos os tipos de vírus herpes simples (1 e 2);
- Herpes Zoster: de modo similar ao que ocorre com o HSV em pacientes com doença pelo HIV, a maioria dos adultos foi previamente infectada pelo vírus varicela zoster, desenvolvendo episódios de herpes zoster frequentes;
- Doenças oportunistas: infecções oportunistas (IO) podem ser causadas por microrganismos não considerados usualmente patogênicos, ou seja, não capazes de desencadear doença em pessoas com sistema imune normal. Entretanto, microrganismos normalmente patogênicos também podem, eventualmente, ser causadores de IO. Nesta situação, as infecções necessariamente assumem um caráter de maior gravidade ou agressividade para serem consideradas oportunistas.
- Vírus: Citomegalovirose, Herpes simples, Leucoencafalopatia Multifocal Progressiva.
- Bactérias: Micobacterioses (tuberculose e complexo Mycobacterium aviumintracellulare), Pneumonias (S. pneumoniae), Salmonelose.
- Fungos: Pneumocistose, Candidíase, Criptococose, Histoplasmose.
- Protozoários: Toxoplasmose, Criptosporidiose, Isosporíase.
- Neoplasias: sarcoma de Kaposi, linfomas não-Hodgkin, neoplasias intra-epiteliais anal e cervical
Sendo assim, são três as classes de ARV habitualmente empregadas na composição do primeiro esquema:
- inibidores da transcriptase reversa análogos de nucleosídeos/nucleotídeos (ITRN/ lTRNt);
- inibidores da transcriptase reversa não-análogos de nucleosideos (ITRNN);
- inibidores da protease potencializados com ritonavir (IP/r).
Os dois ITRN mais empregados na composição do esquema inicial são a zídovudina e a lamivudina (AZT/3TC). Outra dupla considerada de primeira linha é a associação de tenofovir com lamivudina (TDF/3TC). Dois ITRNN podem ser empregados na composição do primeiro esquema ARV no Brasil: o efavirenz (EFV) e a nevirapína (NVP). De um modo geral, o EFV é mais seguro e mais bem tolerado que a NVR sendo, por isso, o ITRNN de escolha na ausência de contraindicações. Os inibidores de protease (IP) são as drogas de segunda linha para associação com a dupla de ITRN/ITRNt na vigência de contraindicações ou intolerância aos ITRNN. Uma vantagem dos IP em relação aos ITRNN é a maior barreira genética dos primeiros, isto é, o HIV precisa adquirir um maior número de mutações genéticas para se tornar resistente aos IP.
Autor
Alisson Ivanski, 25 anos, Acadêmico do 5º período de Medicina, Pontifícia Universidade Católica do Paraná. Formado em Fisioterapia pela Universidade Estadual do Centro-Oeste – UNICENTRO.