Carboidratos são as fontes universais de energia para as células animais e vegetais. A glicose é o carboidrato mais importante neste processo. Nas células, a glicose é degradada ou armazenada por diferentes vias.
Os carboidratos, denominados também como hidratos de carbono, são formados por C, H, e O. Alguns ainda, podem apresentar em sua estrutura o N. Estão relacionados diretamente com o fornecimento de energia para as células e estão presentes em diversos alimentos. Além da função energética, possuem função estrutural, fazem parte do esqueleto vegetal e animal e participam da estrutura dos ácidos nucleicos (RNA e DNA) sob forma de ribose e desoxirribose.
De acordo com a quantidade de átomos de carbono em suas moléculas, os carboidratos podem ser divididos em monossacarídeos, dissacarídeos e polissacarídeos.
Monossacarídeos: ou açucares simples, consistem em uma única unidade cetônica. O mais abundante é o D-glucose (açúcar de 6 carbonos) e é a partir dele que muitos outros são formados. A classificação dos monossacarídeos também pode ser baseada no número de carbonos de suas moléculas; assim, as trioses são os monossacarídeos mais simples, seguidos das tetroses, pentoses, hexoses, heptoses, e assim por diante. São grandes exemplos de monossacarídeos as riboses (pentose), a glicose (hexose), a galactose (hexose), e a frutose (hexose).
Dissacarídeos: conhecidos como glicosídeos, são formados através de uma ligação glicosídica de dois monossacarídeos. Os principais dissacarídeos incluem a sacarose, a lactose e a maltose.
Polissacarídeos: são os açucares mais complexos, macromoléculas formadas pela união de milhares de unidades de monossacarídeos através de ligações glicosídicas, unidas em longas cadeias simples ou ramificadas. São os principais polissacarídeos o amido, o glicogênio e a celulose.
Se inscreva no nosso Canal no Youtube:
Receba dicas que vão mudar sua vida acadêmica e profissional.
1. Metabolismo de Carboidratos
Nos vertebrados, a glicose é transportada através do corpo pelo sangue. Quando as reservas de energia celular estão baixas, a glicose é degradada pela via glicolítica. As moléculas de glicose não necessárias para a imediata produção de energia, são armazenadas como glicogênio no fígado e músculo. Dependendo das necessidades metabólicas da célula, a glicose pode também ser empregada para sintetizar outros monossacarídeos, ácidos graxos e certos aminoácidos.
Os principais carboidratos da dieta são: o amido, a sacarose e a lactose. O glicogênio, a maltose, a glicose livre e a frutose livre constituem frações relativamente menores de carboidratos ingeridos. A absorção dos carboidratos pelas células do intestino delgado é realizada após hidrólise dos dissacarídeos, oligossacarídeos e polissacarídeos em seus componentes monossacarídeos.
As quebras ocorrem sequencialmente em diferentes segmentos do trato gastrointestinal por reações enzimáticas:
Alfa-amilase salivar: a digestão do amido inicia durante a mastigação pela ação α-amilase salivar (ptialina) que hidrolisa as ligações glicosídicas, com a liberação de maltose e oligossacarídeos.
Alfa-amilase pancreática: o amido e o glicogênio são hidrolisados no duodeno em presença da α-amilase pancreática que produz maltose e dextrinas (oligossacarídeos).
Enzimas da superfície intestinal. A hidrólise final da maltose e dextrina é realizada pela maltase e a dextrinase, presentes na superfície das células epiteliais do intestino delgado.
Após a absorção, a glicose no sangue aumenta e as células β das ilhotas pancreáticas secretam insulina que estimula a captação de glicose principalmente pelos tecidos adiposo e muscular.
Nos processos metabólicos dos carboidratos, algumas etapas (vias metabólicas) são essenciais para a obtenção da reserva energética: glicólise (anaeróbia e aeróbia), via das pentoses-fosfato, glicogênese, glicogenólise, gliconeogênese, ciclo de Krebs ou ciclo do ácido cítrico e cadeia respiratória ou fosforilação oxidativa.
1.1. Glicólise
Consiste na oxidação da molécula de glicose formando duas moléculas de ATP e duas moléculas de Ácido Pirúvico. Acontecendo no hialoplasma, é um processo de catabolismo, anaeróbio e aeróbio, universal.
Consiste numa sequência de 10 reações e duas fases: preparatória (compreendem 5 reações nas quais a glicose é fosforilada por dois ATP e convertida em duas moléculas de gliceraldeído−3−fosfato) e de pagamento (as duas moléculas de gliceraldeído−3−fosfato são oxidadas pelo NAD+ e fosforiladas em reação que emprega o fosfato inorgânico. O resultado líquido do processo total de glicólise é a formação de 2 ATP, 2 NADH e 2 piruvato, às custas de uma molécula de glicose).
Em organismos e tecidos aeróbios, em condições aeróbias, o Piruvato é oxidado (com perda do grupo carboxílico) originando o grupo Acetil-CoA que depois é oxidado a CO2 durante o Ciclo de Krebs. Em organismos e tecidos em condições de pouco oxigênio ou em condições anaeróbias, o Piruvato é reduzido a Lactato ou convertido a Etanol + CO2.
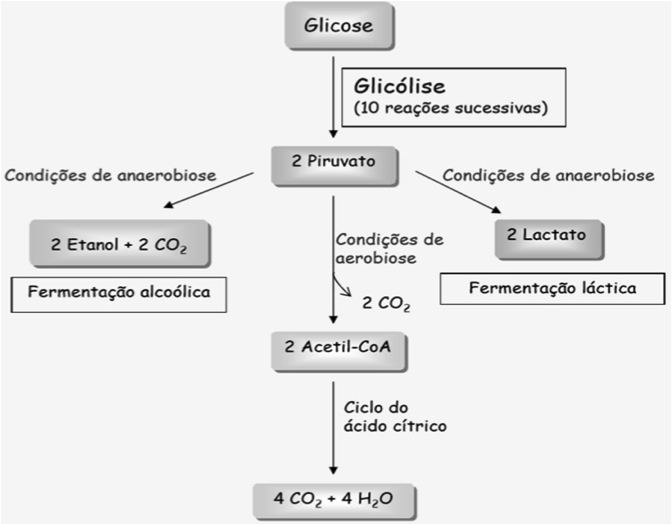
O lactado (proveniente da glicólise anaeróbia) é produzido pelo organismo após a queima da glicose para fornecimento de energia sem a presença de oxigênio. Em atividades físicas de longa duração, por exemplo, o suprimento de oxigênio nem sempre é suficiente. O organismo busca energia em fontes alternativas, produzindo o lactato. O acúmulo desta substância nos músculos pode gerar uma hiperacidez que causa a dor e desconforto logo após o exercício físico.
1.2. Via das pentoses-fosfato
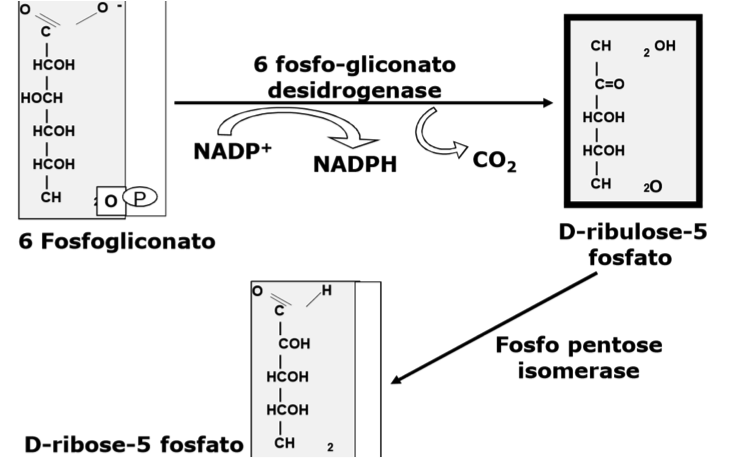
Processos de síntese das pentoses, CO2 e o NADPH, onde, se trata de uma via metabólica alternativa à glicólise para a oxidação da glicose que não requer e não produz ATP.
A via das pentoses-fosfato ocorre no citosol em duas etapas: etapa oxidativa e a etapa não−oxidativa. Na etapa oxidativa a glicose−6−fosfato é convertida à ribulose−5−fosfato acompanhada pela formação de duas moléculas de NADPH. A etapa não−oxidativa envolve a isomerização e condensação de várias moléculas diferentes de açúcar. Três intermediários do processo são utilizados em outras vias: a ribose−5−fosfato, a frutose−6−fosfato e o gliceraldeído−3−fosfato.
Alternativamente, a via das pentoses−fosfato pode ser concebida como um “desvio” para a produção de frutose−6−fosfato a partir da glicose−6−fosfato. Tanto a glicose−6−fosfato como o gliceraldeído−3−fosfato produzidos pela via das pentoses−fosfato podem ser metabolizados a piruvato e, finalmente, oxidado no sistema enzimático mitocondrial.
1.3. Glicogênese
É o processo de síntese do glicogênio a partir da condensação de muitos monômeros de glicose. O glicogênio é armazenado em grânulos intracelulares que também contêm as enzimas que catalisam as reações para a sua síntese e degradação. A glicose armazenada sob a forma de glicogênio no fígado e músculos destinam-se a diferentes funções, como reservatório de glicose à corrente sanguínea e combustível para gerar ATP durante atividade muscular.
Tal processo ocorre logo após a ingestão do alimento, quando os teores de glicose estão elevados na corrente sanguínea. O Lactado é formado nos eritrócitos por glicose é captado pelo fígado e convertido em Glicose-6-fosfato. Após, a glicose−6−fosfato é convertida reversivelmente a glicose−1−fosfato pela fosfoglicomutase e, em presença da UDP−glicose−pirofosforilase, a glicose−1−fosfato reage com a trifosfato de uridina (UTP), para produzir UDP−glicose uma forma “ativada” de glicose.
A unidade glicosil de UDP−glicose é transferida para uma extremidade não−redutora do glicogênio já existente, resultando na anexação de uma nova unidade de glicose. A UDP é reconvertida a UTP à custa de ATP por meio de uma reação de transferência do grupo fosforil catalisada pela nucleosídio−difosfato– cinase.
O glicogênio é uma estrutura amplamente ramificada com pontos de ramificações a cada 8 a 14 resíduos. A ramificação é resultante da ação da enzima amilo-transglicosilase (enzima de ramificação). Essa enzima transfere um fragmento de 6 ou 7 resíduos de glicose, da extremidade não-redutora de uma cadeia para o grupo OH do C6 de uma unidade de glicose na mesma ou em outra cadeia de glicogênio, de modo a formar um enlace onde é estabelecido um ponto de ramificação.
Após a ocorrência de ramificações, unidades de glicose podem ser acrescentadas a partir de resíduos glicosil provenientes da UDP−glicose aos terminais não−redutores de cada uma das cadeias originais ou das ramificações, por meio da glicogênio−sintase. Quando o n° suficiente de unidades são adicionadas, desse modo, ocorrem novas ramificações.
A síntese de glicogênio necessita a existência de uma cadeia de glicogênio já constituída, à qual são adicionados novos resíduos de glicose. Na primeira etapa da síntese, uma glicosil−transferase liga o primeiro resíduo de glicose a um grupo OH de uma proteína chamada glicogenina que atua como molde inicial. Essa, por autocatálise, incorpora novos resíduos de glicose, até formar uma pequena cadeia de até sete resíduos doados pela UDP-glicose, produzindo uma molécula nascente de glicogênio. Nesse ponto, a glicogênio−sintase inicia a síntese do glicogênio, enquanto a glicogenina desliga-se do polímero.
1.4. Glicogenólise
É o processo de conversão do glicogênio em glicose, através da degradação do glicogênio em uma clivagem sequencial de resíduos de glicose a partir das extremidades não-redutoras das ramificações do glicogênio.
A partir do rompimento das ligações pela enzima glicogênio-fosforólise, há a formação do α−D−glicose−1−fosfato. A glicogênio-fosforilase remove unidades sucessivas de glicose ao longo da cadeia até restarem quatro resíduos de um ponto de ramificação. A continuação da degradação ocorre depois da transferência de uma unidade de três resíduos de glicose da ramificação sob a ação da enzima de desramificação do glicogênio, para a extremidade não-redutora de outra ramificação, ou seja, acontece o rompimento de uma ligação com a formação de uma nova ligação. Em sua nova posição, os resíduos de glicose são liberados pela ação da glicogênio-fosforilase.
A remoção do resíduo glicosil restante ligado à cadeia principal é realizada por hidrólise pela mesma enzima de desramificação com a formação de glicose e glicogênio não ramificado. Desse modo, é explicado o aparecimento de pequenas quantidades de glicose livre. O produto final das reações de degradação do glicogênio é a glicose−1−fosfato que é convertida em glicose−6−fosfato pela fosfoglicomutase. A glicose−6−fosfato pode ser utilizada pela glicólise ou pela via das pentoses-fosfato e no fígado, a glicose-6-fosfato também sofre a ação da glicose−6−fosfatase para formar glicose.
1.5. Gliconeogênese
É o processo de formação de novas moléculas de glicose a partir de moléculas menores, como precursores não-glicídicos (lactato, piruvato, glicerol, cadeias carbonadas). Entre as refeições, os teores adequados de glicose sanguínea são mantidos pela hidrólise do glicogênio hepático. Quando o fígado esgota seu suprimento de glicogênio (exemplo, jejum prolongado ou exercício vigoroso), a gliconeogênese fornece a quantidade apropriada de glicose para o organismo.
Considerando o piruvato como ponto inicial da gliconeogênese, as reações podem ser comparadas com as da via glicolítica, porém, no sentido inverso. Muitas das enzimas e intermediários são idênticos. Sete reações são reversíveis, no entanto, três são irreversíveis e devem ser contornadas por meio de outras reações catalisadas por enzimas diferentes.
1.6. Ciclo de Krebs ou Ciclo do Ácido Cítrico
Trata-se de uma via catabolítica cíclica de oxidação total da glicose a CO2 e H2O, com liberação de energia. Tal processo só ocorre em condições aeróbicas, na matriz mitocondrial.
Antes de entrar no ciclo, após a oxidação da molécula de glicose (pelas diversas vias) a Piruvato, este é transportado do citosol até a matriz mitocondrial por uma translocase específica para ser descarboxilado a Acetil-CoA. Para a formação de Acetil-CoA participa do processo o complexo multienzimático piruvato desidrogenase, além de outras enzimas como a CoA-ácido pantotênico e a vitamina B3 (NAD+).
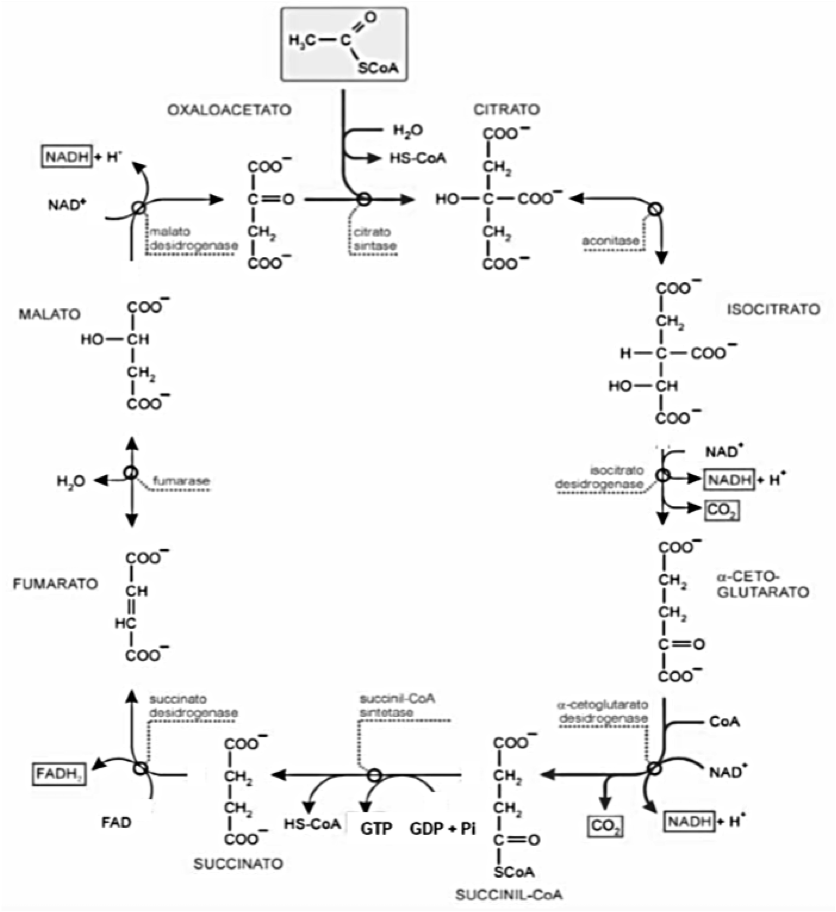
Após formado, o Acetil-CoA entra no ciclo e através de uma reação de condensação com o Oxaloacetato formando o Citrato. A reação é catalisada pela enzima citrato sintetase. Neste processo, há a liberação da coenzima A, que fica livre para atuar na descarboxilação oxidativa de outra molécula de Piruvato e formar uma nova molécula de Acetil-CoA capaz de entrar no ciclo.
Após formado o Citrato, através de uma reação de desidrogenação, este é convertido a Isocitrato via Cis-Aconitato através da enzima aconitase. Trata-se de uma reação reversível.
O Isocitrato sofre de desidrogenação pela ação da enzima isocitrato desidrogenase (enzima ligada à coenzima NAD+) resultando na formação na molécula de Alfa-Cetoglutarato e CO2. Nessa reação irreversível há a liberação de NADH + H+.
Após a formação do Alfa-Cetoglutarato, através de uma reação de descarboxilação oxidativa, o mesmo é oxidado a Succinil-CoA e CO2 pela ação do complexo alfa-cetoglutarato desidrogenase, enzima ligada à coenzima NAD+. Nessa reação irreversível, também há a formação de NADH + H+.
O Succinil-CoA é um composto de alta energia. Fosforila a Guanosina Difosfato (GDP) a Guanosina Trifosfato (GTP) pela ação enzimática da succinil-CoA sintetase. Nesta reação de fosforilação em nível de substrato, ocorre a liberação do Succinato, da coenzima A e a formação de um grupo fosfato terminal de alta energia do GTP a partir de GDP + Pi.
Após a formação do Succinato pela reação reversível, o mesmo passa por uma reação de desidrogenação até a formação da molécula de Fumarato. Tal processo é catalisado pela enzima succinato desidrogenase, a qual contém FAD ligada covalentemente, formando FADH2.
Através da catalização do Fumarato a partir da enzima fumarato desidrogenase (fumarase) e de uma reação reversível de hidratação, há a formação do Malato.
Por fim, na última reação do Ciclo de Krebs ocorre a desidrogenação do malato a Oxaloacetato e o início de um novo ciclo. Esta reação é catalisada pela enzima malato desidrogenase a qual está ligada à coenzima NAD+. Nessa reação reversível, há a formação de NADH + H+.
1.7. Fosforilação Oxidativa
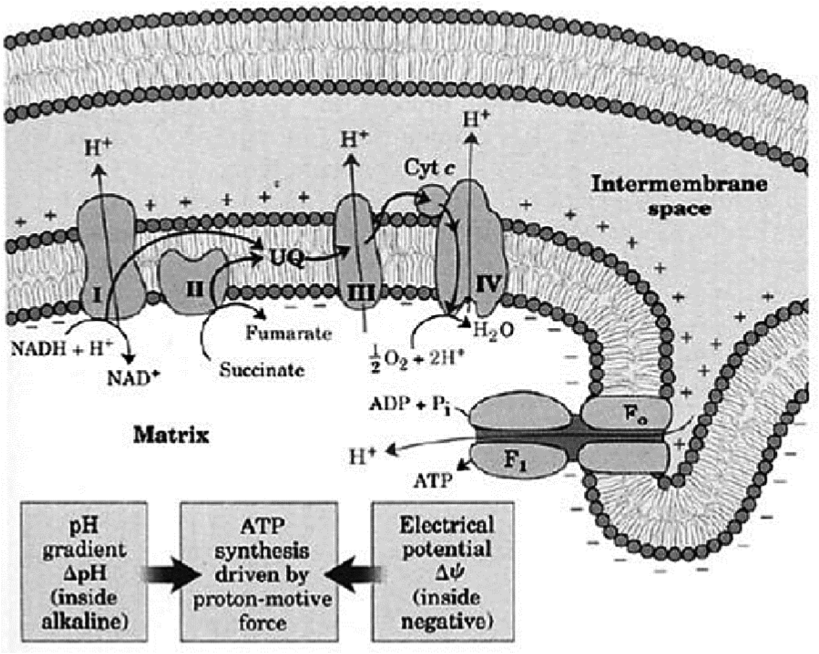
Após o Ciclo de Krebs, este é um processo metabólico de síntese do ATP a partir da energia liberada pelo transporte de elétrons na cadeia respiratória. Ocorrendo nas cristas mitocondriais, é um sistema de transferência de elétrons provenientes do NADH e FADH2 (estas coenzimas são carreadoras do O2, o qual serve como aceptor de H+).
Durante o fluxo de elétrons, há liberação suficiente de energia livre para a síntese de ATP nos sítios de fosforilação oxidativa. Neste fluxo, os elétrons são passados de molécula para molécula nos citocromos presentes nas cristas mitocondriais. Estes “pulam” de um citocromo para outro até chegar no O2 e fazer a liberação de energia convertida em ATP.
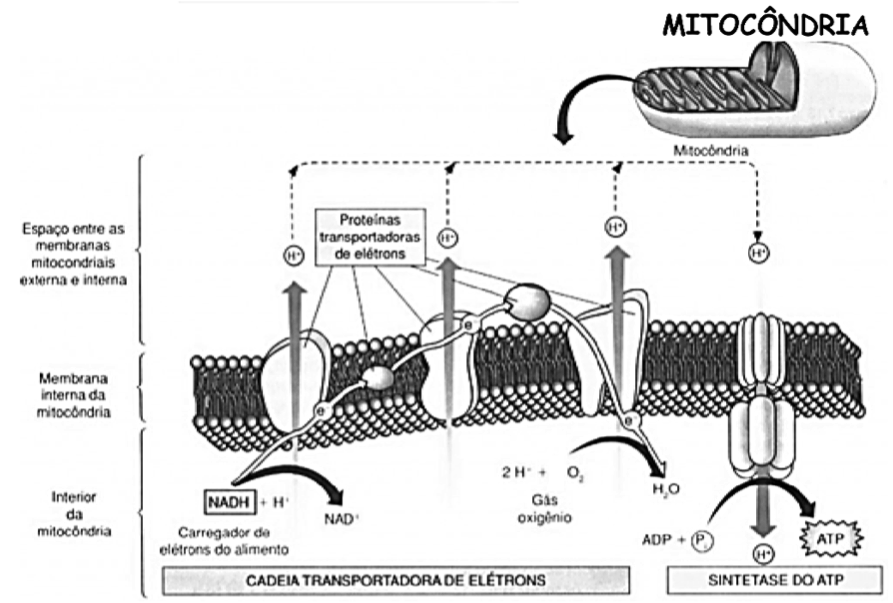
Neste processo, o NADH se liga ao complexo I e transfere seus elétrons para este complexo, iniciando a cadeia de transporte de elétrons. Este complexo é um canal de prótons e bombeia 4 prótons para o espaço intermembranar e transfere elétrons para a ubiquinona (uma proteína inserida na membrana). A ubiniquona transfere os elétrons para o complexo III (bomba de prótons), que bombeia mais 2 prótons para o espaço intermembranar. Os elétrons são transportados pelo complexo III até o citocromo C (que só transfere elétrons) e deste para o complexo IV que além de ser uma bomba de prótons (bombeia 4 prótons) transfere elétrons para o oxigênio reduzindo-o até H2O. Desta maneira, a cada um NADH que inicia esta via, 10 prótons são bombeados para o espaço intermembranar.
O FADH2 possui afinidade ao complexo II, que não é uma bomba de prótons, transfere seus elétrons para a ubiquinona e daí em diante tudo se repete. O FADH2 é responsável pelo bombeamento de 6 prótons para o espaço intermembranar.
Estes prótons retornam através da ATP síntase e são responsáveis pela maior síntese de ATP que acontece na mitocôndria.
1.8. Rendimento total (em ATP) do processo metabólico
A partir da oxidação de uma molécula de glicose durante o metabolismo aeróbico, tem-se um saldo final de 38 ATP.
Na glicólise, através da oxidação de glicose em Ácido Pirúvico há a formação de 2 moléculas de ATP através da fosforilação no nível de substrato e, ainda, com produção de 2 NADH há a formação de 6 moléculas de ATP através da fosforilação oxidativa na cadeia de transporte de elétrons.
Na etapa preparatória, através da formação de Acetil-CoA e produção de 2 NADH há a formação de 6 moléculas de ATP através da fosforilação oxidativa na cadeia de transporte de elétrons.
E por fim, no Ciclo de Krebs, na oxidação de Succinil-CoA a Ácido Succínico ocorre a formação de 2 GTP (equivalentes a ATP) na fosforilação no nível de substrato; 18 ATP através da produção de 6 NADH na fosforilação oxidativa na cadeia transportadora de elétrons e 4 ATP através da produção de 2 FADH2 na fosforilação oxidativa na cadeia de transporte de elétrons.
Mesmo com o saldo teórico final de 38 ATP, na maioria das células eucarióticas, somente há a formação de 36 ATP visto que alguma energia é perdida quando os elétrons são transportados através da membrana mitocondrial, que separa a glicólise (no citoplasma) da cadeia transportadora de elétrons (nas cristas mitocondriais).
Autor: Robson Diego Calixto, acadêmico do curso de odontologia pelo Centro de Ensino Superior dos Campos Gerais – CESCAGE.
Fonte da imagem em destaque: http://thescienceofeating.com
Referências Bibliográficas
– BLACKSTOCK, J. C. Biochemistry. Oxford: Butterworth, 1998.
– LEHNINGER, A. L. Princípios de Bioquímica. 4. ed. São Paulo: Sarvier, 2006.
– STRYER, L. Bioquímica. 4.ed. Rio de Janeiro: Guanabara-Koogan, 1996.
– VOET, D., VOET, J.G., PRATT, C.W. Fundamentos de bioquímica. Porto Alegre: Artmed, 2000.





articulo agregado a favoritos, lo imprimiré cuando llegue a la oficina.